Contatto:Errol Zhou (Sig.)
Telefono: più 86-551-65523315
Cellulare/WhatsApp: più 86 17705606359
QQ:196299583
Skype:lucytoday@hotmail.com
E-mail:sales@homesunshinepharma.com
Aggiungere:1002, Huanmao Edificio, N.105, Mencheng Strada, Hefei Città, 230061, Cina
BioMarin è una società globale di biotecnologie dedicata allo sviluppo e alla commercializzazione di terapie innovative per pazienti con malattie genetiche rare e ultra-rare gravi e potenzialmente letali. Il suo portafoglio di prodotti include 6 prodotti commerciali e una varietà di prodotti Candidate clinici e preclinici. Recentemente, la società ha annunciato che l'Agenzia europea per i medicinali (EMA) ha accettato la domanda di autorizzazione all'immissione in commercio (MAA) per vosoritide (Voxolitide, BMN111).
Vosoritide è un analogo del peptide natriuretico (CNP) di tipo C che viene iniettato una volta al giorno per il trattamento dell'acondroplasia infantile, che è la bassa statura sproporzionata più comune negli esseri umani. Nell'Unione Europea, la revisione MAA è iniziata il 13 agosto. La società prevede ancora di presentare una nuova domanda di farmaco (NDA) per vosoritide alla Food and Drug Administration (FDA) statunitense nel terzo trimestre del 2020. Nell'Unione Europea e negli Stati Uniti, vosoritide ha ottenuto la designazione di farmaco orfano (ODD) per il trattamento dell'acondroplasia.
Se approvato, la vosoritide diventerà il primo farmaco per il trattamento dell'acondroplasia. Il farmaco può trattare la causa principale della malattia e rappresenta un importante passo avanti medico con il potenziale di avere un impatto significativo sui pazienti' vite.

Meccanismo d'azione di vosoritide
L'acondroplasia è la bassa statura sproporzionata più comune negli esseri umani. È caratterizzato da ossificazione endocondrale rallentata, che porta a una brevità sproporzionata e disturbi strutturali delle ossa lunghe, della colonna vertebrale, del viso e della base del cranio. Questa condizione è causata da mutazioni nel gene del recettore 3 del fattore di crescita dei fibroblasti (FGFR3), che è un regolatore negativo della crescita ossea.
Oltre alla statura sproporzionatamente bassa, i pazienti con acondroplasia possono sperimentare gravi complicazioni di salute, tra cui compressione del forame, apnea notturna, gambe piegate, ipoplasia facciale, oscillazioni permanenti della parte bassa della schiena, stenosi spinale e orecchie ricorrenti. Dipartimento di infezione. Alcune di queste complicazioni possono comportare la necessità di un intervento chirurgico invasivo, come la decompressione del midollo spinale e il raddrizzamento delle gambe piegate. Inoltre, studi hanno dimostrato che i tassi di mortalità aumentano per ogni fascia di età.
Vosoritide è un analogo del peptide natriuretico di tipo C (CNP) derivato da peptidi umani naturali ed è un efficace stimolatore dell'ossificazione endocondrale. Il peptide umano naturale è un regolatore positivo della crescita ossea. Vosoritide si lega a recettori specifici e avvia segnali intracellulari che inibiscono la via iperattiva FGFR3.
L'applicazione normativa di vosoritide si basa sui risultati di uno studio globale di fase III randomizzato, in doppio cieco, controllato con placebo, pubblicato a dicembre 2019, e ottiene inoltre i dati di sicurezza ed efficacia a lungo termine dell'espansione in corso di fase II e fase III studi, dati sulla storia delle malattie naturali estesi.
Lo studio globale di fase III ha arruolato 121 bambini con acondroplasia di età compresa tra 5 e 14 anni e le cui piastre di crescita erano ancora aperte, e ha valutato l'efficacia e la sicurezza di vosoritide e placebo. Questi pazienti avevano completato almeno 6 mesi di studio di base prima di entrare nello studio di fase III per determinare i rispettivi tassi di crescita di base. Nello studio di fase III, i pazienti sono stati assegnati in modo casuale a ricevere 52 settimane di vosoritide (15ug / kg / die) o placebo. L'endpoint primario era la variazione del tasso di crescita rispetto al basale nei bambini trattati con vosoritide durante il periodo di trattamento di un anno rispetto al placebo.
I risultati hanno mostrato che lo studio ha raggiunto l'endpoint primario: dopo un anno di trattamento, la variazione del tasso di crescita del trattamento con vosoritide rispetto al basale è stata di 1,6 cm / anno (p< 0,0001)="" dopo="" un="" anno="" di="" trattamento.="" questo="" risultato="" è="" coerente="" con="" i="" risultati="" nell'ampia="" popolazione="" di="" pazienti="" studiata.="" nello="" studio,="" la="" vosoritide="" è="" stata="" generalmente="" ben="" tollerata="" e="" non="" si="" è="" verificato="" un="" calo="" clinicamente="" significativo="" della="" pressione="">
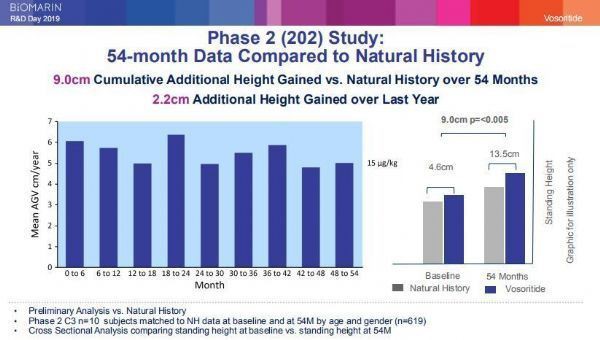
I risultati di uno studio di fase II di scoperta della dose in aperto pubblicato a novembre 2019 hanno mostrato che, rispetto a un nuovo set di dati sull'acondroplasia della storia naturale (n=619), i bambini che hanno ricevuto 15 μg di età e sesso abbinati Nella coorte tre (n=10) pazienti trattati con vosoritide / kg / die, l'altezza media cumulativa è aumentata di 9,0 cm in 54 mesi e i dati erano statisticamente significativi (p< 0,005).="" con="" un="" aumento="" di="" 2,2="" cm="" negli="" ultimi="" 12="" mesi,="" i="" dati="" illustrano="" ulteriormente="" l'effetto="" benefico="" del="" trattamento="" continuo="" con="" vosoritide="">