Contatto:Errol Zhou (Sig.)
Telefono: più 86-551-65523315
Cellulare/WhatsApp: più 86 17705606359
QQ:196299583
Skype:lucytoday@hotmail.com
E-mail:sales@homesunshinepharma.com
Aggiungere:1002, Huanmao Edificio, N.105, Mencheng Strada, Hefei Città, 230061, Cina
Pfizer e Myovant Sciences hanno recentemente annunciato che la Food and Drug Administration (FDA) statunitense ha approvato Myfembree (relugolix40 mg, estradiolo 1,0 mg, noretindrone acetato 0,5 mg), che è una compressa composta di relugolix. È il primo farmaco una volta al giorno per il trattamento della menorragia correlata ai fibromi uterini (HMB) nelle donne in premenopausa. Il trattamento dura fino a 24 mesi.
Nel dicembre 2020, Pfizer e Myovant hanno raggiunto un accordo da 4,2 miliardi di dollari per sviluppare congiuntamente relugolix, un antagonista del recettore dell'ormone di rilascio delle gonadotropine (GnRH). Secondo i termini della cooperazione, Myovant e Pfizer commercializzeranno congiuntamente Myfembree negli Stati Uniti e il prodotto dovrebbe essere lanciato nel giugno 2021.
I fibromi uterini sono una malattia cronica debilitante. I due sintomi più comuni sono menorragia (HMB) e dolore. Negli Stati Uniti, i fibromi uterini colpiscono milioni di donne e ci sono più di 250.000 procedure di isterectomia ogni anno. L'approvazione di Myfembree porterà un trattamento conveniente e non invasivo per le donne con fibromi uterini, prendendo una compressa al giorno e fornendo un sollievo clinicamente significativo per la menorragia.
Vale la pena ricordare che il prodotto composto di AbbVie'Oriahnn (elagolix, estradiolo, noretindrone acetato capsule) è la prima opzione orale non chirurgica per il trattamento della menorragia correlata ai fibromi uterini (HMB) nelle donne in premenopausa. Il farmaco è stato approvato dalla FDA degli Stati Uniti nel maggio 2020. In termini di farmaci, Oriahnn viene assunto per via orale due volte al giorno. Tra i principi attivi del farmaco, elagolix è anche un antagonista orale del recettore del GnRH.
Nel luglio 2018, elagolix (nome commerciale: Orilissa) è stato approvato dalla FDA statunitense per il trattamento del dolore da moderato a severo associato all'endometriosi (EM). Questa approvazione rende Orilissa il primo antagonista orale del recettore del GnRH approvato per il trattamento del dolore da moderato a severo correlato agli EM, ed è anche il primo farmaco orale approvato dalla FDA per il trattamento del dolore da moderato a grave correlato agli EM negli ultimi 10 anni. anni.
Myfembree è stato approvato dalla FDA sulla base dei dati di efficacia e sicurezza di 2 studi di fase 3 (LIBERTY 1, LIBERTY 2). I risultati correlati sono stati pubblicati sulla rivista medica internazionale"New England Journal of Medicine" (NEJM) nel febbraio di quest'anno, con il titolo dell'articolo: Trattamento dei sintomi del fibroma uterino con la terapia combinata Relugolix. Come accennato in precedenza, entrambi gli studi hanno raggiunto l'endpoint primario del sollievo dalla perdita mestruale e allo stesso tempo hanno raggiunto 6 dei 7 principali endpoint secondari. Myfembree ha anche mantenuto una densità ossea paragonabile al placebo, che è una buona resistenza entro 24 settimane. Parte del tema della sicurezza.
I dati specifici sono i seguenti: nei 2 studi, il 72,1% e il 71,2% delle donne nel gruppo Myfembree hanno raggiunto lo standard di remissione alla 24a settimana di trattamento, mentre il gruppo placebo è stato del 16,8% e del 14,7% (entrambi p [GG ] lt;0,0001). La remissione del trattamento è definita come: misurata con il metodo dell'emoglobina alcalina, durante gli ultimi 35 giorni di trattamento, la perdita di sangue mestruale è diminuita di 80 ml rispetto al basale e diminuita di ≥50% rispetto al basale. Nelle pazienti trattate con Myfembree, la perdita di sangue mestruale è diminuita dell'82,0% e dell'84,3% rispetto al basale, rispettivamente (p<0,0001 rispetto="" al="" placebo).="" tra="" i="" pazienti="" trattati="" con="" myfembree,="" le="" reazioni="" avverse="" che="" si="" sono="" verificate="" con="" un="" tasso="" ≥3%="" e="" superiore="" al="" placebo="" includevano:="" vampate,="" sanguinamento="" uterino="" anomalo,="" perdita="" di="" capelli="" e="" diminuzione="" della="" libido.="" in="" questi="" due="" studi,="" non="" è="" stata="" segnalata="" alcuna="" gravidanza="" nel="" gruppo="" di="" trattamento="" con="">
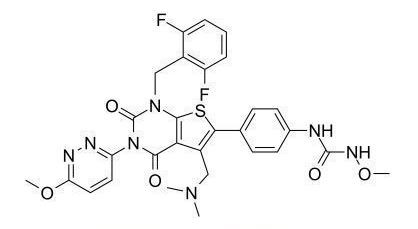
relugolixchimico (fonte della formula strutturale: medchemexpress.com)
Relugolix è un antagonista del recettore dell'ormone di rilascio delle gonadotropine (GnRH), che può ridurre la produzione di estradiolo ovarico bloccando i recettori del GnRH nella ghiandola pituitaria. Questo ormone è noto per stimolare i fibromi uterini e l'utero La crescita dell'endometriosi. Inoltre, relugolix può anche inibire la produzione di testosterone nei testicoli, che può stimolare la crescita delle cellule del cancro alla prostata.
Attualmente, relugolix è in fase di sviluppo per 3 indicazioni terapeutiche: (1) trattamento dei fibromi uterini femminili e dell'endometriosi; (2) trattamento del cancro alla prostata maschile.
relugolix è stato sviluppato da Takeda e Myovant Sciences (una società formata da Roivant e Takeda) ha ottenuto la licenza globale esclusiva nel giugno 2016 ad eccezione del Giappone e di altri paesi asiatici. In Giappone, relugolix è stato approvato nel gennaio 2019 e commercializzato con il marchio Relumina per migliorare i seguenti sintomi causati dai fibromi uterini: menorragia, dolore addominale inferiore, lombalgia e anemia.
mia donna (relugolix40 mg, estradiolo 1,0 mg, noretindrone acetato 0,5 mg) segna il secondo prodotto di Myovant' approvato dalla FDA degli Stati Uniti in meno di 6 mesi nello sviluppo di relugolix. Il 18 dicembre 2020, Orgovyx (relugolix, compresse da 120 mg) è stato approvato dalla FDA per il trattamento di pazienti adulti con carcinoma prostatico avanzato.
Vale la pena ricordare che Orgovyx è il primo e unico antagonista orale del recettore del GnRH approvato dalla FDA statunitense per il trattamento del carcinoma prostatico avanzato. Il farmaco è stato approvato attraverso il processo di revisione prioritaria. Nello studio di fase 3 HERO, il tasso di remissione del trattamento con relugolix è stato del 96,7%, significativamente migliore rispetto a leuprolide acetato (88,8%), riducendo il rischio di eventi avversi cardiovascolari maggiori (MACE) del 54%.
Myovant prevede di presentare una nuova domanda di indicazione per Myfembree alla FDA statunitense nella prima metà del 2021 per il trattamento del dolore da moderato a severo correlato all'endometriosi femminile. Inoltre, sulla base del tasso di inibizione del 100% delle compresse del composto relugolix sull'ovulazione femminile nello studio di fase 1, Myovant e Pfizer hanno avviato uno studio clinico di fase 3 nell'aprile di quest'anno per valutare l'effetto contraccettivo delle compresse del composto relugolix in donne ad alto rischio popolazioni.