Contatto:Errol Zhou (Sig.)
Telefono: più 86-551-65523315
Cellulare/WhatsApp: più 86 17705606359
QQ:196299583
Skype:lucytoday@hotmail.com
E-mail:sales@homesunshinepharma.com
Aggiungere:1002, Huanmao Edificio, N.105, Mencheng Strada, Hefei Città, 230061, Cina
Boehringer Ingelheim ha recentemente annunciato che lo studio clinico globale di fase III InPedILD (NCT04093024) che valuta Ofev (nintedanib) per il trattamento di pazienti pediatrici con malattia polmonare interstiziale (IDL) ha arruolato il primo paziente.
InPedILD è uno studio internazionale di fase III randomizzato, in doppio cieco, controllato con placebo e multicentrico che recluterà pazienti in circa 70 siti di sperimentazione clinica in 24 paesi in tutto il mondo. Lo studio arruolerà bambini e adolescenti (6-17 anni) con fibrosi clinicamente significativa con ILD. Saranno valutate l'esposizione alla dose e la sicurezza di Ofev. Ofev verrà somministrato per via orale per 24 settimane sulla base delle cure di routine, quindi verranno adottate durate diverse. Ofev conduce il trattamento in aperto. Gli endpoint primari erano la concentrazione plasmatica di Ofev&alle settimane 2 e 26 e il numero di pazienti che hanno manifestato TEAE (eventi avversi dovuti al trattamento) alla settimana 24.
Vale la pena ricordare che InPedILD è il primo studio clinico mondiale di&sull'ILD in bambini e adolescenti. Lo studio si basa sullo studio di Fase III INBUILD di Ofev' la supervisione di pazienti adulti con fenotipo progressivo di ILD fibrotico (PF-ILD) Sulla base dell'approvazione, si propone di affrontare le importanti esigenze insoddisfatte dei più vulnerabili popolazione di pazienti pediatrici affetti da ILD.
Child ILD (chILD) comprende più di 200 malattie respiratorie rare che colpiscono neonati, bambini e adolescenti, rendendoli difficili da respirare. In alcuni casi, la fibrosi può svilupparsi in cicatrici e danni ai polmoni. Ciò può avere un impatto importante sulla vita quotidiana delle persone colpite e delle loro famiglie, inclusa un'elevata morbilità e mortalità. Attualmente, non esiste un trattamento approvato per il chILD.
Robin Derting, MD, ricercatore coordinatore dello studio InPedILD e direttore del Respiratory Research Institute presso il Colorado Children's Hospital, ha dichiarato: “Alcuni bambini con ILD possono sviluppare una fibrosi grave e progredirà ulteriormente. Sebbene la fibrosi polmonare nei bambini Le cause sottostanti possono essere diverse, ma siamo felici di determinare se il meccanismo di Ofev&per il trattamento della fibrosi può migliorare la fibrosi polmonare dei bambini&come negli adulti.

Ofev è un inibitore della tirosin chinasi multi-target che può inibire le vie chiave coinvolte nella fibrosi polmonare nella malattia polmonare interstiziale (ILD). Ad oggi Ofev è stato approvato per 3 indicazioni: (1) per il trattamento della fibrosi polmonare idiopatica (IPF); (2) per il trattamento della malattia polmonare interstiziale correlata alla sclerosi sistemica (SSc-ILD); (3)) È usato per trattare altre malattie polmonari interstiziali fibrotiche croniche (PF-ILD) con un fenotipo progressivo oltre a IPF.
Ofev è l'unico farmaco in grado di rallentare il declino della funzione polmonare nei pazienti con SSc-ILD ed è l'unico farmaco approvato per il trattamento della PF-ILD. In Cina, Ofev è stato approvato per il trattamento di IPF e SSc-ILD e la domanda per il trattamento di PF-ILD è stata accettata dalla State Food and Drug Administration alla fine dello scorso anno.
Il dottor Thomas Leonard, direttore esecutivo dello sviluppo clinico e degli affari medici di Boehringer Ingelheim Professional Nursing IPF / ILD, ha dichiarato:" Siamo incoraggiati dai risultati relativi al declino della funzione polmonare di Ofev&nei pazienti con malattia cronica progressiva ILD fibroso (PF-ILD). I nuovi risultati aiutano a sostenere le crescenti prove scientifiche per l'uso di Ofev."
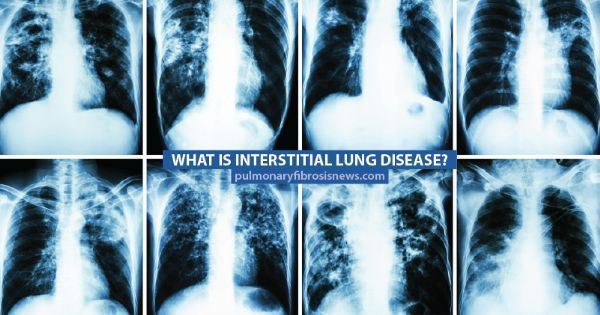
ILD (Fonte immagine: pulmonaryfibrosisnews.com)
Nel luglio di quest'anno, Ofev è stato approvato dall'Unione Europea per il trattamento della PF-ILD. L'approvazione si basa sui risultati dello studio di Fase III INBUILD, che è il primo studio clinico a raggiungere l'endpoint primario in una popolazione di pazienti affetti da ILD. Lo studio è uno studio randomizzato, in doppio cieco, controllato con placebo, a gruppi paralleli, condotto in 153 centri clinici in 15 paesi e ha valutato l'efficacia di Ofev (150 mg, due volte al giorno) per 52 settimane di pazienti con PF-ILD , Sicurezza e tolleranza. Nello studio, sono stati valutati un totale di 663 pazienti, di cui 412 (62,1%) hanno mostrato cambiamenti simili a polmonite interstiziale (UIP) sulla tomografia computerizzata ad alta risoluzione (HRCT). I pazienti sono stati randomizzati in base al pattern di fibrosi rilevato da HRCT e la funzione polmonare è stata valutata in base al tasso annuale di diminuzione della capacità vitale forzata (FVC).
I risultati hanno mostrato che dopo 52 settimane di trattamento, la FVC dei pazienti nel gruppo placebo è diminuita di 188 ml e la FVC dei pazienti nel gruppo Ofev è diminuita di 81 ml. Ciò significa che Ofev ha rallentato il declino della funzione polmonare del 57% (107 ml / anno) rispetto al placebo. In questo studio, il trattamento di Ofev&per ridurre il declino della funzione polmonare è stato coerente in tutti i pazienti, indipendentemente dal pattern di fibrosi alla HRCT, ed era coerente con i risultati del trattamento di Ofev' s di IPF e SSc-ILD pazienti. In particolare, nei pazienti con fibrosi simile all'UIP sottoposti a terapia ormonale sostitutiva, i risultati hanno mostrato che rispetto al placebo, il trattamento con Ofev ha ridotto il declino della funzione polmonare del 61% (128,2 ml / anno).
In questo studio, Ofev è stato associato a una diminuzione numerica del rischio di esacerbazione o morte rispetto al placebo. Il beneficio del trattamento è anche accompagnato da una riduzione dei risultati riportati dai pazienti (come dispnea e tosse). La sicurezza osservata in questo studio è coerente con gli studi clinici su IPF e SSc-ILD. L'evento avverso più comune è stata la diarrea. L'incidenza del gruppo di trattamento Ofev e del gruppo placebo è stata rispettivamente del 66,9% e del 23,9%.