Contatto:Errol Zhou (Sig.)
Telefono: più 86-551-65523315
Cellulare/WhatsApp: più 86 17705606359
QQ:196299583
Skype:lucytoday@hotmail.com
E-mail:sales@homesunshinepharma.com
Aggiungere:1002, Huanmao Edificio, N.105, Mencheng Strada, Hefei Città, 230061, Cina
Galderma è la più grande azienda di dermatologia globale indipendente al mondo e leader nella ricerca e nello sviluppo di soluzioni dermatologiche scientificamente definite e provate dal punto di vista medico. Recentemente, l'azienda ha annunciato che i risultati completi di uno studio di fase II (NCT03181503) di nemolizumab per il trattamento del prurito nodolo moderato a grave (prurigo nodularis, PN) in pazienti adulti sono stati pubblicati nel New England Journal of Medicine (NEJM). Titolo dell'articolo: Prova di Nemolizumab in Prurigo Nodularis da moderato a grave.
PN è una malattia cronica pruriginosa della pelle con lesioni cutanee nodiulali multiple. Si tratta di una malattia della pelle cronica rara, potenzialmente fatale. I noduli di pelle spessi coprono una vasta area del corpo e sono associati a forti prurito. La malattia spesso causa gravi danni alla qualità della vita. Nemolizumab è un anticorpo monoclonale di prima classe che può colpire il recettore interleuchina 31 (IL-31R) e bloccare la segnalazione IL-31. L'IL-31 è una citochina che induce prurito e la sua segnalazione svolge un ruolo chiave nella patogenesi del PN.
Nel mese di novembre 2019, la Us Food and Drug Administration (FDA) ha concesso a nemolizumab una qualifica di farmaco innovativo (BTD) per il trattamento del prurito legato al PN. Galderma si sta preparando attivamente a lanciare il progetto chiave di fase III della monoterapia nemolizumab per pazienti adulti con PN nel 2020.
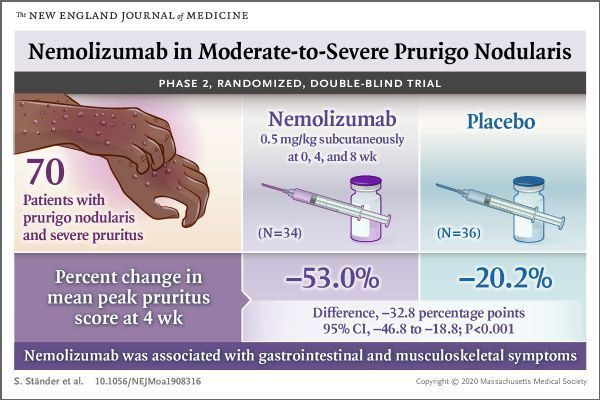
Lo studio pubblicato in NEJM è uno studio randomizzato, doppio cieco, controllato con placebo, parallelo, multi-centro, 12 settimane di fase II. Un totale di 70 adulti con PN da moderato a grave e prurito grave sono stati arruolati pazienti. Nello studio, dalla linea di base alla settimana 8, i pazienti sono stati assegnati casualmente a ricevere un'iniezione sottocutanea di nemolizumab (dose: 0,5 mg / kg di peso corporeo) o placebo ogni 4 settimane. Settimana 0 (linea di base), settimana 4, e settimana 8, rispettivamente Una iniezione sotto la pelle. In questo studio, il prurigo nodulare da moderato a grave è stato definito come avente 20 o più noduli, e il prurito grave è stato definito come il punteggio medio dell'intensità del prurito più grave sulla scala numerica di valutazione di almeno 7 punti (intervallo di punteggio da 0 [Nessun prurito] a 10 [il prurito più grave che si possa immaginare]).
I risultati hanno mostrato che lo studio ha raggiunto il punto finale primario: dalla linea di base alla settimana 4, rispetto al gruppo placebo, il punteggio della scala di valutazione numerica pruriginosa di picco (PP-NRS) del gruppo di trattamento nemolizumab è stato significativamente ridotto rispetto alla linea di base. Il punteggio base PP-NRS dei 2 gruppi è stato di 8,4. Alla settimana 4, il punteggio PP-NRS del gruppo di trattamento di nemolizumab è diminuito di 4,5 punti rispetto al basale (variazione: -53,0%) e il gruppo placebo è diminuito di 1,7 punti (cambiamento: -20,2%). I dati presentavano differenze statisticamente significative (variazione:- 32,8%; 95% CI: -46,8 a -18,8, p<0.001). in="" addition,="" in="" all="" other="" indicators,="" the="" nemolizumab="" treatment="" group="" showed="" significant="" differences.="" at="" week="" 18="" (10="" weeks="" after="" the="" last="" dose),="" 38%="" of="" patients="" in="" the="" nemolizumab="" treatment="" group="" completely="" cleared="" or="" nearly="" completely="" cleared="" pn,="" compared="" with="" 6%="" in="" the="" placebo="" group="" (p="0.001)." in="" the="" study,="" nemolizumab="" was="" well="" tolerated,="" and="" no="" imbalance="" of="" adverse="" events="" was="" observed="" between="" the="" two="" groups.="" nemolizumab="" treatment="" is="" associated="" with="" gastrointestinal="" symptoms="" (abdominal="" pain="" and="" diarrhea)="" and="" musculoskeletal="">
Dr. Thibaud Portal, capo globale dei farmaci da prescrizione a Galderma, ha detto: "È ben noto che il prurito nodulare ha un grave impatto negativo sulla qualità della vita dei pazienti. Nonostante un gran numero di esigenze non soddisfatte, attualmente non esiste un piano di trattamento registrato. Questa fase II I risultati dello studio indicano che il nemolizumab può svolgere un ruolo chiave nei pazienti con prurito nodolare da moderato a grave. Siamo impegnati a testare ulteriormente questo farmaco in uno studio di fase III e siamo determinati a fornire soluzioni per i pazienti con prurito nodiardo. "
Nemolizumab è un anticorpo monoclonale umanizzato che si rivolge al recettore IL-31 A e si ritiene che inibisti l'attività biologica di IL-31 bloccando in modo competitivo il legame di IL-31 al suo recettore. nemolizumab è stato sviluppato da Sino-foreign Pharmaceuticals. Nel 2016, Galderma ha ottenuto i diritti globali (esclusi Giappone e Taiwan) di nemolizumab dalle licenze farmaceutiche sino-estere. Nemolizumab è stato creato utilizzando ACT-Ig, una tecnologia proprietaria di ingegneria anticorpale di Sinopharm, che può estendere l'emivita biologica degli anticorpi nel sangue. (Bioon.com)